Teorema ekuipartisi
Dalam mekanika statistika klasik, teorema ekuipartisi adalah sebuah rumusan umum yang merelasikan temperatur suatu sistem dengan energi rata-ratanya. Teorema ini juga dikenal sebagai hukum ekuipartisi, ekuipartisi energi, ataupun hanya ekuipartisi. Gagasan dasar teorema ekuipartisi adalah bahwa dalam keadaan kesetimbangan termal, energi akan terdistribusikan secara merata ke semua bentuk-bentuk energi yang berbeda; contohnya energi kinetik rata-rata per derajat kebebasan pada gerak translasi sebuah molekul haruslah sama dengan gerak rotasinya.
Teorema ekuipartisi mampu memberikan prediksi-prediksi yang kuantitatif. Seperti pada teorema virial, teorema ekuipartisi dapat memberikan hasil perhitungan energi kinetik dan energi potensial rata-rata total suatu sistem pada satu temperatur tertentu, yang darinya kapasitas kalor sistem dapat dihitung. Namun, teorema ekuipartisi juga memberikan nilai rata-rata komponen individual energi tersebut, misalnya energi kinetik suatu partikel ataupun energi potensial suatu dawai. Contohnya, teorema ini dapat memberikan prediksi bahwa setiap molekul dalam suatu gas ideal monoatomik memiliki energi kinetik rata-rata sebesar (3/2)kBT dalam kesetimbangan termal, dengan kB adalah tetapan Boltzmann dan T adalah temperatur. Secara umum, teorema ini dapat diterapkan ke semua sistem-sistem fisika klasik yang berada dalam kesetimbangan termal tak peduli seberapa rumitnya sekalipun sistem tersebut. Teorema ekuipartisi dapat digunakan untuk menurunkan hukum gas ideal dan hukum Dulong-Petit untuk kapasitas kalor jenis benda padat. Teorema ini juga dapat digunakan untuk memprediksi sifat dan ciri bintang-bintang, bahkan berlaku juga untuk katai putih dan bintang neutron, karena teorema ini berlaku pula ketika efek-efek relativitas diperhitungkan.
Walaupun teorema ekuipartisi memberikan prediksi yang sangat akurat pada kondisi-kondisi tertentu, teorema ini menjadi tidak akurat ketika efek-efek kuantum menjadi signifikan, misalnya pada temperatur yang sangat rendah. Ketika energi termal kBT lebih kecil daripada perjarakan energi kuantum pada suatu derajat kebebasan, energi rata-rata dan kapasitas kalor dari derajat kebebasan ini akan lebih kecil daripada nilai energi yang diprediksi oleh teorema ekuipartisi. Derajat kebebasan ini dikatakan menjadi "beku" ketika energi termal lebih kecil daripada perjarakan energi kuantum ini. Contohnya, kapasitas kalor suatu benda padat akan menurun pada temperatur rendah seiring dengan membekunya berbagai jenis gerak yang dimungkinkan. Hal ini berlawanan dengan prediksi teorema ekuipartisi yang memprediksikan nilai kapasitas kalor yang konstan. Fenomena menurunnya kapasitas kalor ini memberikan tanda awal bagi para fisikawan abad ke-19 bahwa fisika klasik tidaklah benar dan diperlukan model ilmiah baru yang lebih akurat dalam menjelaskan fenomena ini. Selain itu, teorema ekuipartisi juga gagal dalam memodelkan radiasi benda hitam (juga dikenal sebagai bencana ultraviolet). Hal ini mendorong Max Planck untuk mencetuskan gagasan bahwa energi yang dipancarkan oleh suatu objek terpancarkan dalam bentuk terkuantisasi. Hipotesis revolusioner ini kemudian memacu perkembangan mekanika kuantum dan teori medan kuantum.
Konsep dasar[sunting | sunting sumber]

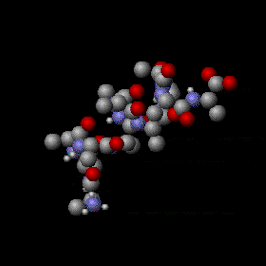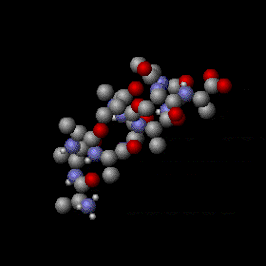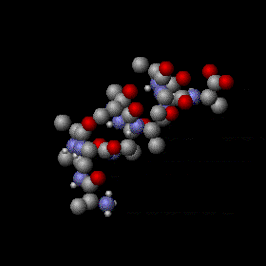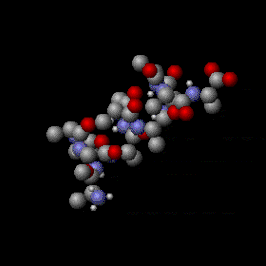
Kata "ekuipartisi" berarti "terbagi secara merata". Kata ini diturunkan dari bahasa Latin æquus ("setara atau sama rata"), dan partitionem ("pembagian, porsi").[1][2] Konsep awal ekuipartisi adalah bahwa energi kinetik total suatu sistem akan terdistribusikan secara merata ke semua bentuk-bentuk energinya (dilihat secara rata-rata), seketika sistem tersebut telah mencapai kesetimbangan termal. Teorema ekuipartisi juga memberikan prediksi kuantitatif bentuk-bentuk energi ini. Contohnya, teorema ini memprediksikan bahwa tiap atom gas mulia yang berada dalam kesetimbangan termal T memiliki energi kinetik translasi sebesar (3/2)kBT, dengan kB adalah tetapan Boltzmann. Sebagai konsekuensinya, oleh karena energi kinetik sama dengan 1/2*mass*kecepatan^2, atom yang lebih berat seperti xenon akan memiliki kecepatan rata-rata yang lebih lambat daripada atom yang lebih ringan seperti helium pada temperatur yang sama. Gambar di samping menunjukkan distribusi Maxwell-Boltzmann kecepatan atom dari keempat gas mulia tersebut.
Energi translasi dan gas ideal[sunting | sunting sumber]
Energi kinetik suatu partikel bermassa m dan berkecepatan v adalah
dengan vx, vy dan vz adalah komponen Kartesius dari kecepatan v. Di sini, H adalah Hamiltonian dan digunakan sebagai simbol energi karena formalisme Hamiltonian memainkan peran pusat dalam perumusan umum teorema ekuipartisi.
Oleh karena energi kinetika bersifat kuadratis terhadap komponen-komponen kecepatan, berdasarkan prinsip kedistribusian merata (ekuipartisi), ketiga komponen ini akan memberikan kontribusi sebesar ½kBT terhadap energi kinetik rata-rata pada kesetimbangan termal. Sehingga energi kinetik rata-rata partikelnya adalah (3/2)kBT, sebagaimana yang diberikan pada contoh gas mulia di atas.
Secara umumnya, pada gas ideal, total energinya hanya terdiri dari energi kinetik (translasional) berdasarkan asumsi bahwa partikel-partikel gas tersebut bergerak secara independen dari satu sama lainnya dan tidak memiliki derajat kebebasan internal. Teorema ekuipartisi memprediksikan bahwa energi total rata-rata suatu gas ideal berpartikel sejumlah N adalah (3/2) N kB T.
Selanjutnya kapasitas kalor gas adalah (3/2) N kB, dan sehingganya kapasitas kalor satu mol partikel gas ideal tersebut adalah (3/2)NAkB = (3/2)R, dengan NA adalah tetapan Avogadro dan R adalah tetapan gas. Oleh karena R ≈ 2 cal/(mol·K), teorema ekuipartisi memprediksikan bahwa kapasitas kalor molar gas ideal adalah kira-kira 3 cal/(mol·K). Prediksi ini telah berhasil dikonfirmasikan melalui eksperimen.[3]
Energi kinetik purata memungkinkan kita juga untuk menghitung kecepatan akar purata kuadrat vrms dari partikel gas:
dengan M = NAm adalah massa satu mol partikel gas. Hasil turunan ini dapat diterapkan ke dalam hukum Graham mengenai efusi.[4]
Energi rotasi dan pergulingan molekul dalam larutan[sunting | sunting sumber]
Mirip dengan contoh di atas, molekul yang berotasi sesuai dengan prinsip momen inersia I1, I2 dan I3 memiliki energi rotasi sebesar
dengan ω1, ω2, dan ω3 adalah komponen kecepatan sudut. Dengan prinsip yang sama pada kasus translasi sebelumnya, teorema ekuipartisi mengharuskan bahwa dalam kesetimbangan termal, energi rotasi rata-rata tiap partikel adalah (3/2)kBT. Teorema ini juga memungkinkan kita menghitung kecepatan sudut rata-rata molekul.[5]
Energi potensial dan osilator harmonik[sunting | sunting sumber]
Teorema ekuipartisi juga berlaku kepada energi potensial. Contohnya pada osilator harmonik seperti dawai yang memiliki energi potensial kuadratik
dengan a menunjukkan kekakuan dawai dan q adalah penyimpangan dari kesetimbangan. Jika sistem berdimensi satu ini bermassa m, maka energi kinetik H-nya adalah
dengan v dan p = mv menunjukkan kecepatan dan momentum osilator. Dengan menggabungkan kedua persamaan di atas akan menghasilkan energi total[6]
Teorema ekuipartisi mengyiratkan bahwa pada kesetimbangan termal, osilator memiliki energi rata-rata
dengan tanda kurung menunjukkan rata-rata dari nilai yang dikurungkan.[7]
Hasil penurunan ini berlaku untuk segala jenis osilator harmonik, misalnya pada bandul, molekul yang bergetar, maupun pada osilator elektronik pasif. Menggunakan teorema ekuipartisi, tiap-tiap osilator menerima energi total rata-rata kBT dan sehingganya berkonrtibusi sebesar kB terhadap kapasitas kalor sistem tersebut. Hal ini kemudian dapat digunakan untuk menurunkan rumus derau Johnson–Nyquist[8] dan hukum Dulong–Petit untuk kapasitas kalor benda padat.

Kapasitas kalor jenis benda padat[sunting | sunting sumber]
Salah satu penerapan teorema ekuipartisi yang penting adalah untuk menurunkan kapasitas kalor jenis benda kristal padat. Tiap-tiap atom pada benda padat ini dapat berosilasi ke tiga arah secara bebas dan independen, sehingga padatan dapat dipandang sebagai sistem yang memiliki 3N osilator harmonik sederhana, dengan N menunjukkan jumlah atom dalam kekisi kristal tersebut. Oleh karena tiap osilator harmonik memiliki energi rata-rata kBT, energi total rata-rata padatan itu adalah sebesar 3NkBT, dan kapasitas kalornya adalah 3NkB.
Dengan mengambil nilai N sebagai tetapan Avogadro NA, dan menggunakan hubungan R = NAkB antara tetapan gas R dengan tetapan Boltzmann kB, hal ini akan menjelaskan hukum Dulong-Petit mengenai kapasitas kalor jenis benda padat, yang menyatakan bahwa kapasitas kalor jenis (per satuan massa) suatu benda padat berbanding terbalik terhadap bobot atomnya. Dalam versi modernya, kapasitas kalor molar suatu benda padat adalah 3R ≈ 6 cal/(mol·K).
Namun, hukum ini menjadi tidak akurat pada temperatur yang rendah. Hal ini disebabkan oleh efek-efek kuantum. Selain itu, hukum ini juga tidak konsisten dengan hukum ketiga termodinamika, yang menurutnya kapasitas kalor molar zat apapun haruslah menuju nilai nol seiring dengan temperatur sistem menuju nol mutlak.[8] Teori yang lebih akurat kemudian dikembangkan oleh Albert Einstein (1907) dan Peter Debye (1911) dengan memasukkan pertimbangan efek-efek kuantum.[9]
Sedimentasi partikel[sunting | sunting sumber]
Energi potensial tidaklah selalu bersifat kuadratis. Teorema ekuipartisi menunjukkan bahwa jika derajat kebebasan x hanya berkontribusi sebesar xs terhadap energinya, maka dalam kesetimbangan termal, rata-rata energi bagian tersebut adalah kBT/s.
Contoh penerapan turunan ini misalnya pada sedimentasi partikel-partikel yang disebabkan oleh gravitasi.[10] Bir dapat menjadi kabur disebabkan oleh gumpalan protein yang menghamburkan cahaya.[11] Lama kelamaan, gumpalan-gumpalan ini akan bergerak menuju dasar tabung oleh karena gravitasi. Walau demikian, partikel juga dapat berdifusi melawan gaya gravitasi dan seketika kesetimbangan antara keduanya tercapai, teorema ekuipartisi dapat digunakan untuk menentukan posisi rata-rata suatu gumpalan partikel tertentu yang bermassa apung mb. Untuk sebuah botol bir yang tinggi botolnya tak terhingga, energi potensial gravitasi dirumuskan
dengan z adalah ketinggian gumpalan protein dalam botol dan g adalah percepatan gravitasi. Oleh karena s = 1, rata-rata energi potensial suatu gumpalan protein adalah sama dengan kBT. Sehingganya, suatu gumpalan protein dengan massa apung 10 MDa (kira-kira sebesar virus) akan mengakibatkan kaburan dengan tinggi rata-rata sekitar 2 cm pada kesetimbangan. Proses sedimentasi menuju kesetimbangan ini dapat dihitung menggunakan persamaan Mason-Weaver.[12]
Perumusan umum teorema ekuipartisi[sunting | sunting sumber]
Bentuk paling umum teorema ekuipartisi menyatakan bahwa di bawah asumsi tertentu, pada suatu sistem fisik yang berfungsi energi Hamiltonian H dan berderajat kebebasan x, persamaan ekuipartisi berikut akan berlaku pada kesetimbangan termal untuk semua indeks m dan n:[5][7][10]
δmn di sini merupakan delta Kronecker, yang nilainya sama dengan satu apabila m = n atau nol apabila sebaliknya. Tanda kurung pererataan diasumsikan sebagai rerata ensembel atas ruang fase ataupun, di bawah asumsi ergodisitas, sebagai rata-rata waktu suatu sistem tunggal.
Teorema ekuipartisi umum ini berlaku baik pada ensembel mikrokanonis,[7] yakni ketika energi total sistemnya adalah konstan, maupun pada ensembel kanonis,[5][13] yakni ketika sistemnya tersambung kepada penangas kalor yang dapat bertukar energi.
Rumusan umum di atas setara dengan dua rumus berikut:
Apabila derajat kebebasan xn hanya memiliki suku kuadratis anxn2 pada Hamiltonian H, maka rumus pertama di atas mengimplikasikan
yang nilainya dua kali lebih besar daripada kontribusi yang diberikan oleh derajat kebebasan ini terhadap energi rata-rata . Sehingga teorema ekuipartisi untuk sistem yang memiliki energi kuadratis akan mudah diturunkan dari rumus umum di atas. Dengan argumen yang sama, apabila 2 digantikan dengan s, rumus di atas berlaku untuk energi bentuk anxns.
Derajat kebebasan xn adalah koordinat-koordinat dalam ruang sistem dan umumnya dibagi lagi ke dalam koordinat posisi rampatan gk dan koordinat momentum rampatan pk, dengan pk adalah momentum konjugat terhadap qk. Pada situasi ini, rumus pertama di atas berarti bahwa untuk semua k,
Menggunakan persamaan mekanika Hamiltonian,[6] rumus ini dapat juga ditulis sebagai
Dengan cara yang sama, menggunakan rumus kedua
dnm
Hubungan dengan teorema virial[sunting | sunting sumber]
Teorema ekuipartisi umum adalah perpanjangan dari teorema virial (yang diajukan pada tahun 1870[14]), yang menyatakan bahwa
dengan t adalah waktu.[6] Perbedaan antara kedua teorema ini adalah teorema virial menghubungkan penjumlahan rata-rata energi total terhadap satu sama lainnya daripada rata-rata energi individual pada teorema ekuipartisi. Teorema virial juga tidak menghubungkan penjumlahan energi ini terhadap temperatur T. Selain itu, penurunan teorema virial biasanya diekspresikan sebagai rata-rata energi terhadap waktu, sedangkan pada teorema ekuipartisi, penurunannya diekspresikan sebagai rata-rata energi terhadap ruang fase.
Penerapan teorema ekuipartisi[sunting | sunting sumber]
Hukum gas ideal[sunting | sunting sumber]
Teorema ekuipartisi dapat diterapkan untuk menurunkan rumus gas ideal. Berawal dari persamaan
untuk menghitung rata-rata energi kinetik per partikel. Teorema ekuipartisi dapat digunakan untuk menurunkan hukum gas ideal dari mekanika klasik.[5] Jika q = (qx, qy, qz) dan p = (px, py, pz) menandakan vektor letak dan momentum partikel gas, dan F adalah resultan gaya pada partikel, maka
di mana kesamaan pertama adalah hukum kedua Newton, dan kesamaan kedua menggunakan persamaan Hamilton dan rumus ekuipartisi. Dengan mentotalkan seluruh sistem yang berpartikel N akan menghasilkan:

Menurut hukum ketiga Newton dan asumsi bahwa gas berperilaku ideal, resultan gaya yang bekerja pada suatu sistem bergas ideal akan bermuasal dari gaya yang diterapkan oleh dinding penampung gas. Gaya ini kemudian bermanifestasi sebagai tekanan gas P. Sehingga
dengan dS adalah luas infinitesimal permukaan dinding penampung. Oleh karena divergensi vektor letak q adalah
maka menutur teorema divergensi
dengan dV adalah volume infinitesimal penampung dan V adalah total volume penampunga.
Dengan menggabungkan kedua persamaan ini akan didapatkan
yang secara langsung memberikan persamaan gas ideal berpartikel N:
dengan n = N/NA adalah jumlah mol gas dan R = NAkB adalah tetapan gas. Walaupun teorema ekuipartisi memberikan contoh penurunan hukum gas ideal yang simpel, hasil yang sama juga dapat diturunkan menggunakan metode alternatif seperti fungsi partisi.[15]
Gas diatomik[sunting | sunting sumber]
Sebuah partikel gas diatomik dapat dimodelkan sebagai dua massa m1 dan m2 yang dihubungkan oleh pegas dengan konstanta Hooke a. Pemodelan ini disebut sebagai pendekatan rotor tegar osilator harmonik.[16] Sistem ini akan memiliki energi sebesar
dengan p1 dan p2 adalah momentum dua atom dan q adalah deviasi jarak antar dua atom pada kesetimbangannya. Tiap derajat kebebasan energi ini bersifat kuadratik dan sehingganya haruslah berkontribusi sebesar ½kBT terhadap energi rata-rata total dan ½kB terhadap kapasitas kalornya. Sehingga kapasitas kalor gas bermolekul diatomik sebanyak N akan diprediksikan bernilai sebesar 7N·½kB (momentum p1 dan p2 masing-masing berkontribusi sebanyak tiga derajat kebebasan dan q berkontribusi satu derajat kebebasan). Selanjutnya pula, kapasitas kalor satu mol molekul diatomik akan memiliki (7/2)NAkB = (7/2)R dan sehingganya kapasitas kalor molarnya haruslah kira-kira 7 cal/(mol·K). Namun nilai kapasitas kalor molar yang didapatkan dari hasil percobaan biasanya berkisar sebesar 5 cal/(mol·K)[17] dan menurun menjadi 3 cal/(mol·K) pada temperatur yang sangat rendah.[18] Ketidakcocokan antara hasil prediksi berdasarkan teorema ekuipartisi dengan nilai hasil percobaan ini tidak dapat dijelaskan menggunakan model molekul yang lebih kompleks oleh karena dengan menambahkan lebih banyak derajat kebebasan hanya akan meningkatkan kalor jenis yang diprediksi.[19] Ketidakcocokan ini kemudian menjadi bukti nyata diperlukannya perlakuan teori kuantum untuk menyelesaikan masalah ini.

Gas ideal pada kondisi relativistik ekstrem[sunting | sunting sumber]
Teorema ekuipartisi yang digunakan di atas untuk menurunkan hukum gas ideal berdasarkan mekanika Newton klasik tidak dapat digunakan apabila efek-efek relativitas menjadi dominan dalam sistem yang dikaji, seperti misalnya katai putih dan bintang neutron.[7] Oleh karenanya persamaan gas ideal harus dimodifikasi. Teorema ekuipartisi memungkinkan kita untuk dengan mudah menurunkan hukum gas ideal yang berlaku pada kondisi relativistik ekstrem.[5] Pada kasus ini, energi kinetik suatu partikel tunggal adalah sebesar
Dengan menurunkan H terhadap px akan menghasilkan rumus
Penurunan yang sama terhadap py dan pz akan menghasilkan rumus yang sama dan dengan menambahkan ketiganya akan menghasilkan
dengan kesamaan terakhir mengikuti rumus ekuipartisi. Sehingganya energi total rata-rata pada sistem gas relativistik ekstrem adalah dua kali lebih besar daripada energi total rata-rata gas non-relativistik. Untuk gas relativistik berpartikel N, nilai energinya adalah 3 NkBT.
Gas non-ideal[sunting | sunting sumber]
Dalam kasus gas ideal, partikel-partikel gas diasumsikan hanya berinteraksi secara tumbukan. Teorema ekuipartisi dapat pula digunakan untuk menurunkan energi dan tekanan "gas non-ideal" yang partikel-partikelnya dapat berinteraksi melalui gaya-gaya konservatif yang potensial U(r)-nya bergantung hanya pada jarak r antar partikel.[5] Ini dapat dideskripsikan secara sederhana dengan pertama-tama menyempitkan fokus kita pada satu partikel tunggal gas dan melakukan pendekatan pada gas-gas lainnya menggunakan distribusi simetri bola. Kemudian, dengan menggunakan fungsi distribusi radial g(r) sehingganya rapatan probabilitas menemukan partikel lainnya dalam ruang lingkup r dari suatu partikel adalah sama dengan 4πr2ρg(r), dengan ρ = N/V adalah rapatan rata-rata atau massa jenis rata-rata gas.[20] Energi potensial rata-rata kemudian berhubungan dengan interaksi partikel tunggal tersebut dengan gas lainnya dan secara matematis diekspresikan sebagai
Energi potensial rata-rata total gas oleh karenanya adalah , dengan N adalah jumlah partikel dalam gas dan faktor ½ diperlukan karena penjumlahan keseluruhan partikel akan membuat interaksi antar partikel yang diperhitungkan dihitung dua kali. Dengan menambahkan energi kinetik dan potensial, dan menerapakn teorema ekuipartisi, kita akan mendapatkan persamaan energi
Dengan cara yang sama,[5] kita juga dapat menurunkan persamaan tekanan sebagai
Osilator anharmonik[sunting | sunting sumber]
Osilator anharmonik (berbeda dengan osilator harmonik sederhana) memiliki energi potensial yang bukan kuadratis pada ekstensi q (posisi umum yang mengukur penyimpangan sistem dari kesetimbangan). Osilator seperti ini dapat memberikan kita gambaran komplementer terhadap teorema ekuipartisi.[21][22] Contoh-contoh yang sederhana dapat diberikan menggunakan fungsi energi potensial berbentuk
dengan C dan s adalah tetapan bilangan real sembarang. Dalam hal ini, hukum ekuipartisi memprediksi bahwa
Sehingga, energi potensial rata-rata sama dengan kBT/s, dan bukannya kBT/2 seperti yang ada pada osilator harmonik kuadratis (s = 2).
Lebih umumnya, suatu fungsi energi berdimensi satu memiliki ekpansi Taylor pada ekstensi q:
untuk bilangan integer non-negatif n. Ketiadaan suku n = 1 dikarenakan ketiadaan gaya resultan sehingga turunan pertama energinya adalah nol. Suku n = 0 tidak perlu dimasukkan karena energi pada posisi kesetimbangan secara konvensi ditentukan sebagai nol. Dalam kasus ini, hukum ekuipartisi memprediksi bahwa[21]
Berlawanan dengan contoh-contoh lainnya, rumus ekuipartisi
tidak mengizinkan energi potensial rata-rata ditulis dalam tetapan-tetapan yang diketahui.
Gerak Brown[sunting | sunting sumber]

Teorema ekuipartisi dapat digunakan untuk menurunkan gerak Brown suatu partikel dari persamaan Langevin.[5] Menurut persamaan Langevin, gerak suatu partikel bermassa m dan berkecepatan v ditentukan oleh hukum Newton kedua
dengan F'rnd adalah gaya acak yang mewakili osilasi acak partikel dan molekul-molekul disekitarnya; tetapan waktu τ mewakili gaya seret yang melawan gerak partikel dalam larutan. Gaya seret sering ditulis sebagai Fdrag = −γv; sehingga tetapan waktu τ sama dengan m/γ.
Perkalian bintik (skalar) dari persamaan ini dengan vektor posisi r, setelah dirata-ratakan akan menghasilkan persamaan
untuk gerak Brown (dikarenakan gaya acak Frnd tidak berkorelasi dengan posisi r). Dengan menggunakan identitas matematika
dan
persamaan dasar gerak Brown dapat ditransformasikan menjadi
dengan kesamaan terakhir mengikuti teorema ekuipartisi untuk energi kintetik translasional:
Persamaan diferensial di atas untuk (dengan kondisi-kondisi awal yang sesuai) dapat diselesaikan secara eksak:
Dalam skala waktu yang singkat, t << τ, partikel berperilaku sebagai partikel yang bergerak bebas: berdasarkan deret Taylor fungsi eksponensial, jarak kuadrat bertambah kira-kira kuadratis:
Namun dalam skala waktu yang panjang, t >> τ, suku konstan dan eksponensialnya menjadi dapat diabaikan, sehingga jarak kuadrat bertambah hanya secara linear:
Hal ini menjelaskan difusi partikel seiring dengan berjalannya waktu.
Fisika bintang[sunting | sunting sumber]
Teorema ekuipartisi dan teorema virial yang berkaitan dengannya telah lama digunakan dalam bidang astrofisika.[23] Sebagai contohnya, teorema virial dapat digunakan untuk memperkirakan temperatur bintang atau limit Chandrasekhar massa katai putih.[24][25]
Temperatur rata-rata suatu bintang dapat diperkirakan dari teorema ekuipartisi.[26] Karena kebanyakan bintang bersimetri bulat, total energi potensial gravitasionalnya dapat diperkirakan menggunakan pengintegralan
dengan M(r) adalah massa beradius r dan ρ(r) adalah kepadatan bintang pada jari-jari r; G mewakili tetapan gravitasi dan R adalah jari-jari total bintang. Dengan mengasumsikan bahwa kepadatan bintang konstan di segala jari-jari, pengintegralan ini menghasilkan rumus
dengan M adalah massa total bintang. Sehingganya energi potensial rata-rata partikel tunggal adalah
dengan N adalah jumlah partikel dalam bintang. Dikarenakan bintang-bintang pada umumnya mayoritas terdiri dari hidrogen, N secara kasar sama dengan M/mp, dengan mp adalah massa satu proton. Penerapan teorema ekuipartisi ini memberikan nilai perkiraan temperatur bintang
Dengan mansubstitusikan massa dan radius Matahari akan kita dapatkan temperatur surya kira-kira T = 14 juta kelvin, sangat dekat dengan temperatur inti 15 juta kelvin. Namun, Matahari lebih kompleks daripada model asumsi yang kita pakai. Baik temperatur dan kepadatannya bervariasi tergantung pada jari-jarinya, sehingga nilai yang cukup sesuai yang didapatkan di atas (7% galat relatif) sebagiannya hanya disebabkan oleh keberuntungan saja.[27]
Pembentukan bintang[sunting | sunting sumber]
Rumus yang sama dapat diterapkan untuk menentukan kondisi-kondisi pembentukan bintang dalam awan molekul raksasa.[28] Fluktuasi lokal dalam rapatan awan tersebut dapat menyebabkan kondisi tak terkontrol dan cepat di mana awan tersebut runtuh karena gravitasinya sendiri. Keruntuhan seperti itu terjadi ketika teorema ekuipartisi ataupun teorem virial tidak lagi berlaku, yakni ketika energi potensial gravitasionalnya melebih dua kali energi kinetik.
Dengan berasumsi bahwa kepadatan awan ρ
menghasilkan massa minimum yang diperlukan untuk kontraksi bintang, massa Jeans MJ
Dengan mensubstitusikan nilai-nilai yang pada umumnya terpantau pada awan tersebut (T = 150 K, ρ = 2×10−16 g/cm3) kita dapatkan massa minimum perkiraan sebesar 17 massa surya, yang konsisten dengan pembentukan bintang terpantau. Efek ini dikenal juga sebagai instabilitas Jeans, dinamakan setelah fisikawan Britania James Hopwood Jeans yang mempublikasikannya pada tahun 1902.[29]
Turunan[sunting | sunting sumber]
Energi kinetik dan distribusi Maxwell–Boltzmann[sunting | sunting sumber]
Perumusan awal teorema ekuipartisi menyatakan bahwa, dalam segala sistem fisik apapun yang berada dalam kesetimbangan termal, setiap partikelnya memiliki energi kinetik rata-rata yang persis sama (eksak), (3/2)kBT.[30] Hal ini dapat ditunjukkan menggunakan distribusi Maxwell–Boltzmann, yang merupakan distribusi probabilitas
untuk kecepatan partikel bermassa m dalam sistem, di mana kecepatan v adalah magnitudo dari kecepatan vektor
Distribusi Maxwell–Boltzmann berlaku untuk segala sistem yang terdiri dari atom, dan mengasumsikan hanya ensembel kanonis, secara spesifiknya, bahwa energi kinetik terdistribusi menurut faktor Boltzmannya pada temperatur T.[30] Energi kinetik rata-rata suatu partikel bermassa m diberikan oleh rumus integral
sebagaimana yang dinyatakan oleh teorema ekuipartisi. Hasil yang sama juga dapat didapatkan dengan mereratakan energi partikel menggunakan probabilitas penemuan partikel pada keadaan energi kuantum tertentu.[15]
Energi kuadratik dan fungsi partisi[sunting | sunting sumber]
Lebih umumnya, teorema ekuipartisi menyatakan bahwa segala derajat kebebasan x yang muncul dalam energi total H hanya sebagai suku kuadratik sederhana Ax2, dengan A adalah tetapan konstan, memiliki energi rata-raata ½kBT dalam kesetimbangan termal. Dalam hal ini teorema ekuipartisi dapat diturunkan dari fungsi partisi Z(β), dengan β = 1/(kBT) adalah temperatur invers kanonis.[31] Pengintegralan terhadap variabel x menghasilkan
dalam rumus untuk Z. Energi rata-rata yang diasosiasikan dengan faktor ini adalah
sebagaimana yang dinyatakan oleh teorema ekuipartisi.
Pembuktian umum[sunting | sunting sumber]
Penurunan umum teorema ekuipartisi dapat ditemukan dalam banyak buku teks mekanika statistika, baik untuk ensembel mikrokanonis[5][7] dan untuk ensembel kanonis.[5][13] Keduanya melibatkan pererataan terhadap ruang fase sistem yang merupakan manifold simplektik.
Untuk menjelaskan penurunan-penurunan ini, notasi berikut digunakan. Pertama, ruang fase dideskripsikan menurut koordinat posisi rampatan qj bersamaan dengan momentum konjugatnya pj. Kuantitas qj secara penuh mendeskripsikan konfigurasi sistem, manakala kuantitas (qj,pj) secara bersama mendeskripsikan secara penuh keadaannya.
Kedua, volume infinitesimal
dari ruang fase diperkenalan dan digunakan untuk mendefinisikan volume Γ(E, ΔE) porsi bagian ruang fase di mana energi H sistem berada di antara dua limit, E dan E + ΔE:
Dalam ekspresi ini, ΔE diasumsikan sangat kecil, ΔE << E. Dengan cara yang sama, Σ(E) didefinisikan sebagai volume total ryang fase di mana energinya lebih kecil daripada E:
Karena ΔE sangat kecil, pengintegralan berikut ini memenuhi kesamaan
di mana elips-elips tersebut mewakili integran (yang diintegralkan). Dari sini, Γ proposional terhadap ΔE
dengan ρ(E) adalah rapatan keadaan. Berdasarkan definisi mekanika statistik, entropi S sama dengan kB log Σ(E), dan temperatur T didefinisikan sebagai
Ensembel kanonis[sunting | sunting sumber]
Dalam ensembel kanonis, sistem berada dalam kesetimbangan termal dengan penangas kalor tak terhingga bertemperatur T (dalam kelvin).[5][13] Probabilitas tiap-tiap keadaan dalam ruang fase sistem diberikan oleh faktor Boltzmann dikalikan dengan faktor normalisasi , yang dipilih sedemikiannya penjumlahan probabilitas-probabilitasnya adalah satu
di mana β = 1/kBT. Pengintegralan parsial untuk suatu variabel ruang fase xk (yang dapat berupa qk ataupun pk) antara dua limit a dan b menghasilkan persamaan
di mana dΓk = dΓ/dxk, yakni, pengintegralan pertamanya tidak dilakukan terhadap xk. Suku pertamanya biasanya nol, baik dikarenakan xk adalah nol pada limit ataupun energinya menuju tak terhingga pada limit-limit tersebut. Dalam hal itu teorema ekuipartisi untuk ensembel kanonisnya mengikuti
Di sini, simbol pererataan adalah rata-rata ensembel yang dilakukan terhadap ensembel kanonis.
Ensembel mikrokanonis[sunting | sunting sumber]
Dalam ensembel mikrokanonis, sistem terisolasi dari lingkungan luar, atau paling tidak, terhubung sangat sedikit dari dunia luar.[7] Sehingga, energi totalnya secara efektif konstan; lebih cermatnya, kita mengatakan bahwa energi total H terperangkap antara E dan E+dE. Untuk suatu energi E dan penyimpangannya dE, terdapat suatu daerah ruang fase Γ di mana sistem tersebut memiliki energi tersebut, dan probabilitas tiap-tiap keadaan dalam daerah ruang fase adalah sama, menurut definisi ensembel mikrokanonis. Berdasarkan definisi ini, rata-rata ekuipartisi variabel ruang fase xm (yang dapat berupa qk ataupun pk) dan xn diberikan oleh rumus
di mana kesamaan terakhir dibenarkan karena E adalah konstan sehingga ia tidak tergantung pada xn. Pengintegralan parsialnya akan menghasilkan relasi
karena suku pertama pada sisi kanan adalah nol.
Substitusi hasil ini kepada persamaan sebelumnya akan menghasilkan
Karena , maka:
Sehingga kita telah menurunkan perumusam umum teorema ekuipartisi.
yang sangat berguna dalam penerapan-penerapan seperti pada contoh-contoh di atas.
Lihat pula[sunting | sunting sumber]
Catatan dan referensi[sunting | sunting sumber]
- ^ "equi-". Online Etymology Dictionary. Diakses tanggal 2008-12-20.
- ^ "partition". Online Etymology Dictionary. Diakses tanggal 2008-12-20..
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamakundt_1876 - ^ Fact Sheet on Uranium Enrichment U.S. Nuclear Regulatory Commission. Accessed 30 April 2007
- ^ a b c d e f g h i j k Pathria, RK (1972). Statistical Mechanics. Pergamon Press. hlm. 43–48, 73–74. ISBN 0-08-016747-0.
- ^ a b c Goldstein, H (1980). Classical Mechanics (edisi ke-2nd.). Addison-Wesley. ISBN 0-201-02918-9.
- ^ a b c d e f Huang, K (1987). Statistical Mechanics (edisi ke-2nd). John Wiley and Sons. hlm. 136–138. ISBN 0-471-81518-7.
- ^ a b Mandl, F (1971). Statistical Physics. John Wiley and Sons. hlm. 213–219. ISBN 0-471-56658-6.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamapais_1982 - ^ a b Tolman, RC (1918). "A General Theory of Energy Partition with Applications to Quantum Theory". Physical Review. 11 (4): 261–275. Bibcode:1918PhRv...11..261T. doi:10.1103/PhysRev.11.261.
- ^ Miedl M, Garcia M, Bamforth C (2005). "Haze formation in model beer systems". J. Agric. Food Chem. 53 (26): 10161–5. doi:10.1021/jf0506941. PMID 16366710.
- ^ Mason, M (1924). "The Settling of Small Particles in a Fluid". Physical Review. 23 (3): 412–426. Bibcode:1924PhRv...23..412M. doi:10.1103/PhysRev.23.412.
- ^ a b c Tolman, RC (1938). The Principles of Statistical Mechanics. New York: Dover Publications. hlm. 93–98. ISBN 0-486-63896-0.
- ^ Clausius, R (1870). "Ueber einen auf die Wärme anwendbaren mechanischen Satz". Annalen der Physik. 141: 124–130. (Jerman)
Clausius, RJE (1870). "On a Mechanical Theorem Applicable to Heat". Philosophical Magazine, Ser. 4. 40: 122–127. - ^ a b L. Vu-Quoc, Configuration integral (statistical mechanics) Diarsipkan 2012-04-28 di Wayback Machine., 2008.
- ^ McQuarrie, DA (2000). Statistical Mechanics (edisi ke-revised 2nd). University Science Books. hlm. 91–128. ISBN 978-1-891389-15-3.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaWueller_1896 - ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaEucken_1912 - ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamamaxwell_1875 - ^ McQuarrie, DA (2000). Statistical Mechanics (edisi ke-revised 2nd). University Science Books. hlm. 254–264. ISBN 978-1-891389-15-3.
- ^ a b Tolman, RC (1927). Statistical Mechanics, with Applications to Physics and Chemistry. Chemical Catalog Company. hlm. 76–77.
- ^ Terletskii, YP (1971). Statistical Physics (edisi ke-translated: N. Fröman). Amsterdam: North-Holland. hlm. 83–84. ISBN 0-7204-0221-2. LCCN 70157006.
- ^ Collins, GW (1978). The Virial Theorem in Stellar Astrophysics. Pachart Press.
- ^ Chandrasekhar, S (1939). An Introduction to the Study of Stellar Structure. Chicago: University of Chicago Press. hlm. 49–53. ISBN 0-486-60413-6.
- ^ Kourganoff, V (1980). Introduction to Advanced Astrophysics. Dordrecht, Holland: D. Reidel. hlm. 59–60, 134–140, 181–184.
- ^ Chiu, H-Y (1968). Stellar Physics, volume I. Waltham, MA: Blaisdell Publishing. LCCN 6717990 Periksa nilai
|lccn=(bantuan). - ^ Noyes, RW (1982). The Sun, Our Star. Cambridge, MA: Harvard University Press. ISBN 0-674-85435-7.
- ^ Ostlie, DA; Carroll BW (1996). An Introduction to Modern Stellar Astrophysics. Reading, MA: Addison–Wesley. ISBN 0-201-59880-9.
- ^ Jeans, JH (1902). "The Stability of a Spherical Nebula". Philosophical Transactions of the Royal Society A. 199 (312–320): 1–53. Bibcode:1902RSPTA.199....1J. doi:10.1098/rsta.1902.0012.
- ^ a b McQuarrie, DA (2000). Statistical Mechanics (edisi ke-revised 2nd). University Science Books. hlm. 121–128. ISBN 978-1-891389-15-3.
- ^ Callen, HB (1985). Thermodynamics and an Introduction to Thermostatistics. New York: John Wiley and Sons. hlm. 375–377. ISBN 0-471-86256-8.
Bacaan lebih lanjut[sunting | sunting sumber]
- Huang, K (1987). Statistical Mechanics (edisi ke-2nd). John Wiley and Sons. hlm. 136–138. ISBN 0-471-81518-7.
- Khinchin, AI (1949). Mathematical Foundations of Statistical Mechanics (G. Gamow, translator). New York: Dover Publications. hlm. 93–98. ISBN 0-486-63896-0.
- Landau, LD (1980). Statistical Physics, Part 1 (edisi ke-3rd). Pergamon Press. hlm. 129–132. ISBN 0-08-023039-3.
- Mandl, F (1971). Statistical Physics. John Wiley and Sons. hlm. 213–219. ISBN 0-471-56658-6.
- Mohling, F (1982). Statistical Mechanics: Methods and Applications. John Wiley and Sons. hlm. 137–139, 270–273, 280, 285–292. ISBN 0-470-27340-2.
- Pathria, RK (1972). Statistical Mechanics. Pergamon Press. hlm. 43–48, 73–74. ISBN 0-08-016747-0.
- Pauli, W (1973). Pauli Lectures on Physics: Volume 4. Statistical Mechanics. MIT Press. hlm. 27–40. ISBN 0-262-16049-8.
- Tolman, RC (1927). Statistical Mechanics, with Applications to Physics and Chemistry. Chemical Catalog Company. hlm. 72–81. ASIN B00085D6OO
- Tolman, RC (1938). The Principles of Statistical Mechanics. New York: Dover Publications. hlm. 93–98. ISBN 0-486-63896-0.
Pranala luar[sunting | sunting sumber]
- Applet demonstrating equipartition in real time for a mixture of monatomic and diatomic gases Diarsipkan 2020-08-06 di Wayback Machine.
- The equipartition theorem in stellar physics, written by Nir J. Shaviv, an associate professor at the Racah Institute of Physics in the Hebrew University of Jerusalem.

































































![{\displaystyle \Gamma (E,\Delta E)=\int _{H\in \left[E,E+\Delta E\right]}d\Gamma .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c1d30011a6e9f81ffb1ec8d5f853eb11512962c8)

![{\displaystyle \int _{H\in \left[E,E+\Delta E\right]}\ldots d\Gamma =\Delta E{\frac {\partial }{\partial E}}\int _{H<E}\ldots d\Gamma ,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/dacf6f8ccd4ccf04ffa00683a62e9327772e5f0f)




![{\displaystyle {\mathcal {N}}\int \left[e^{-\beta H(p,q)}x_{k}\right]_{x_{k}=a}^{x_{k}=b}d\Gamma _{k}+{\mathcal {N}}\int e^{-\beta H(p,q)}x_{k}\beta {\frac {\partial H}{\partial x_{k}}}d\Gamma =1,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4e941a978fe3d56ab99364c732bd077bb21eee1e)


![{\displaystyle {\begin{aligned}{\Bigl \langle }x_{m}{\frac {\partial H}{\partial x_{n}}}{\Bigr \rangle }&={\frac {1}{\Gamma }}\,\int _{H\in \left[E,E+\Delta E\right]}x_{m}{\frac {\partial H}{\partial x_{n}}}\,d\Gamma \\&={\frac {\Delta E}{\Gamma }}\,{\frac {\partial }{\partial E}}\int _{H<E}x_{m}{\frac {\partial H}{\partial x_{n}}}\,d\Gamma \\&={\frac {1}{\rho }}\,{\frac {\partial }{\partial E}}\int _{H<E}x_{m}{\frac {\partial \left(H-E\right)}{\partial x_{n}}}\,d\Gamma ,\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aaed7c2b326b93b2548e32655ffc2945954a1b23)




